ニュースレター Vol.5
はじめに
皆さん、いかがお過ごしでしょうか?今回は、近い将来承認されるかもしれない重水素化医薬品の候補物質のお話をしたいと思います。現在までにFDAが承認した重水素化医薬品は、ハンチントン舞踏病治療薬デューテトラベナジンのみですが、ブリストル・マイヤーズスクイブ(株)が開発中のDeucravacitinib (BMS-986165)は、乾癬患者を対象とした有効性及び安全性を検討するプラセボ及び実薬対照試験(第三相試験)において、優越性が認められたことが報告されており、承認される日が近いかもしれません。
Deucravacitinibは、Nメチル基が重水素化された小分子JAK阻害剤です(J. Med. Chem. 2019, 62, 8973-8995.)。JAKはヤヌスキナーゼ(Janus kinase)の略称で、JAK1、JAK2、JAK3、TYK2の4種類があります。Deucravacitinibは、TYK2に対する高い選択性を有し、TYK2偽キナーゼ(JH2)ドメインを標的化するアロステリック阻害剤です。これまでの小分子JAK阻害剤は、触媒活性部位であるJH1ドメインを標的としているため、あるキナーゼのみを選択的に阻害させることが難しく、副作用発現の懸念がありました。Deucravacitinibは、高親和性JH2リガンドであり、経口治療薬として開発された最初の偽キナーゼ指向型治療薬です。詳しい情報がまだ入手できていませんが、元々、重水素医薬品として開発されているようで、テトラベナジンとデューテトラベナジンのように、対になる軽水素医薬品がありません。このことは、重水素化がリード化合物最適化の一つの手段としての地位を確立してきたと言えるのかもしれません。今後の動向が楽しみです。(同志社女子大学・前川 京子)
第3回 Deut-Switchセミナー開催報告
2021年7月16日 (火) 14:00~16:45に、オンラインにて、第3回 Deut-Switchセミナーを開催いたしました(図1)。公開セミナーとして研究班内外に周知した結果、開催日当日までに33名の参加登録があり、質疑応答では活発な議論がなされました。演者は、A01班及びA02班に関連した話題として、宮本 寛子先生(愛知工業大学)、馬場 正昭先生(神戸大学分子フォトサイエンス研究センター・横浜市立大学)をお迎えし、これまでの研究成果をご紹介いただきました。簡単ではありますが、本セミナーの内容につきましてニュースレターでご紹介させていただきます。

1,『ベンゼン分子の重水素化効果-高分解能レーザー分光と ab initio 計算- 』 馬場 正昭 先生
馬場 正昭先生は、1979年京都大学大学院理学研究科修士課程を修了された後、分子科学研究所文部技官、神戸大学理学部助手、京都大学教養部・総合人間学部助教授、京都大学大学院理学研究科教授を経て、現在は神戸大学分子フォトサイエンス研究センター、及び横浜市立大学に所属されています(図2)。本セミナーでは、ベンゼン分子の重水素化効果を高分解能レーザー分光とab initio 計算により決定した研究成果(J. Chem. Phys. 2011, 135, 054305.)を中心にお話しいただきました。

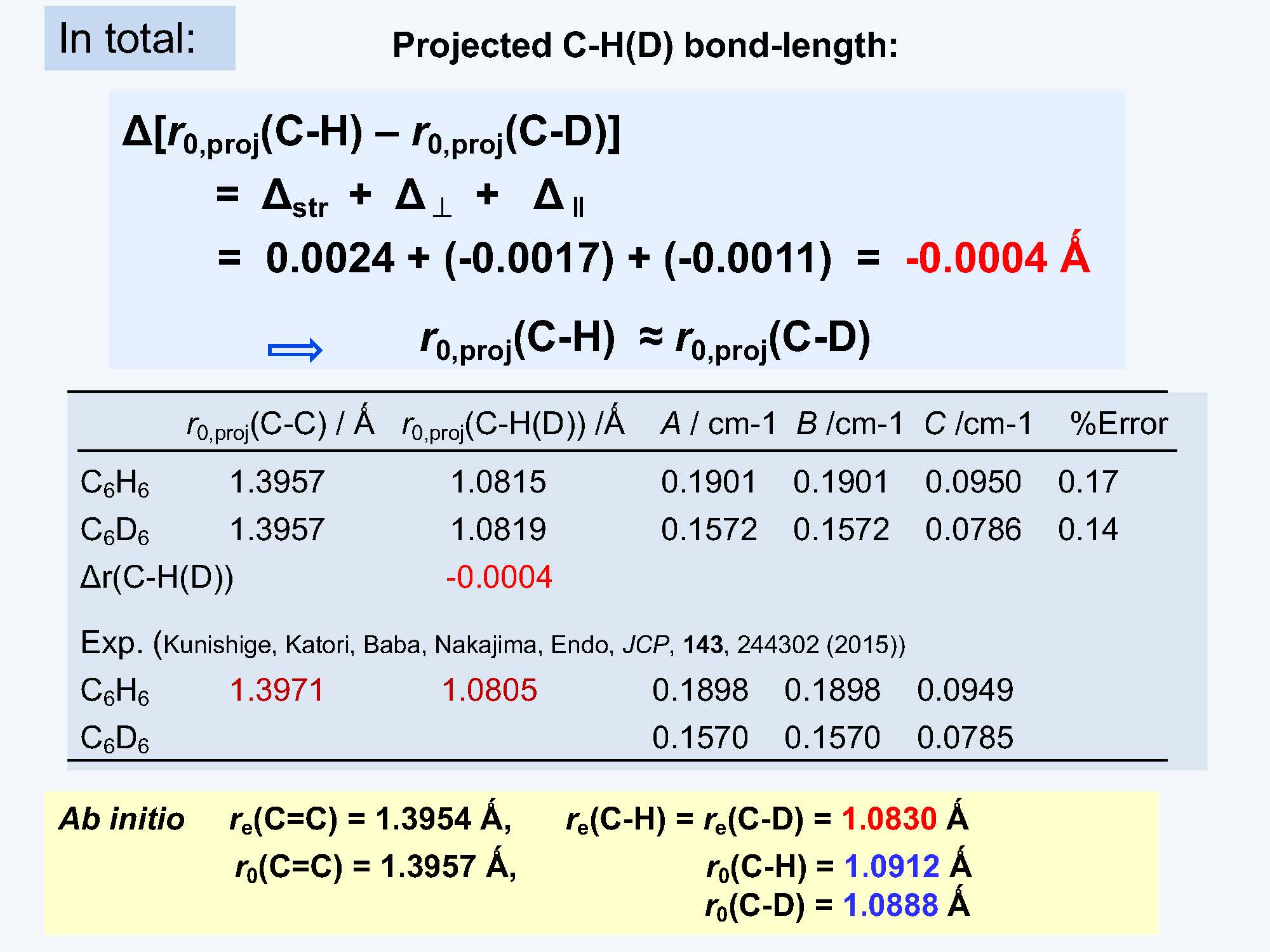
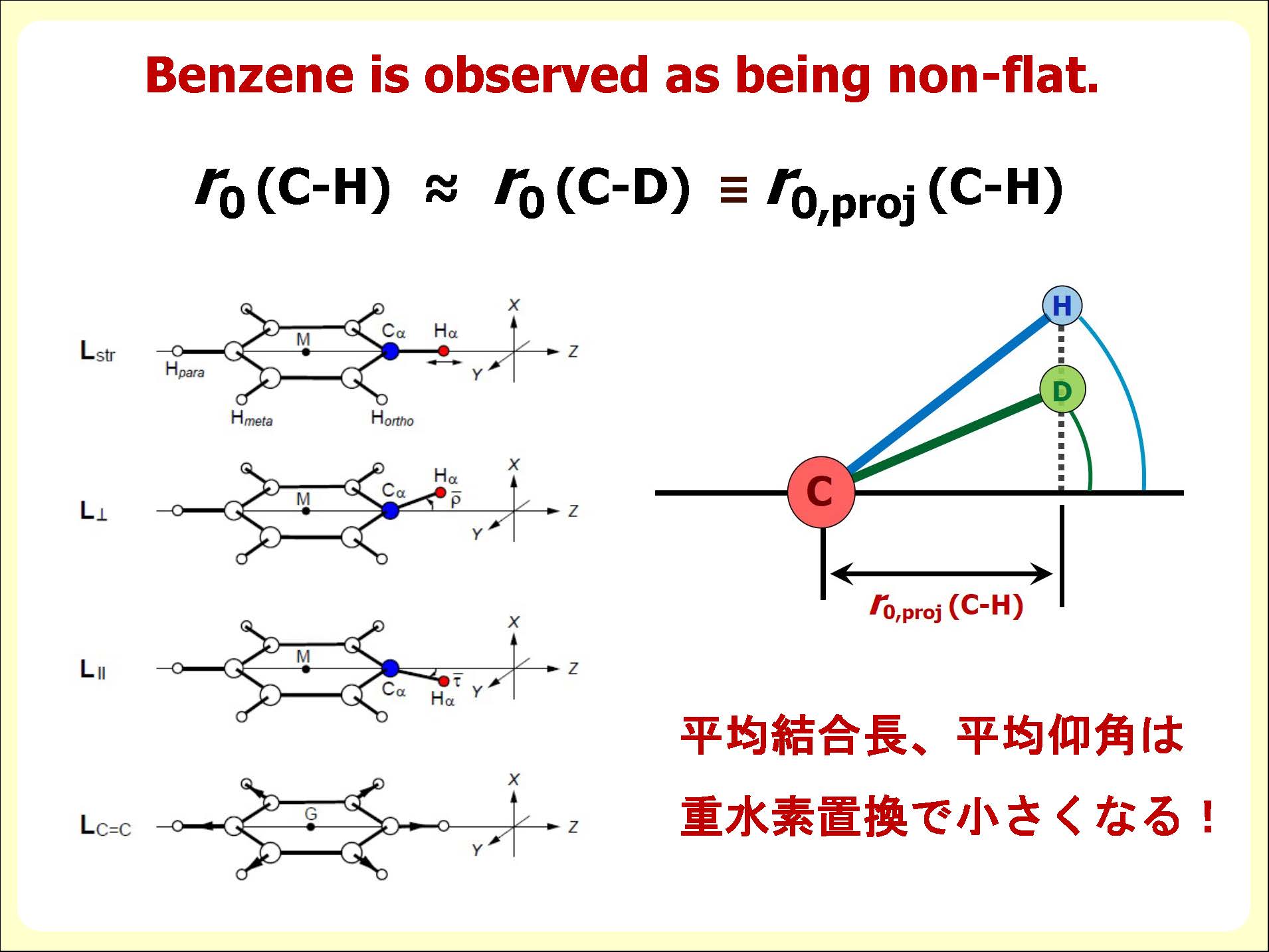
ベンゼン分子は、基底状態では平面で六角形であるとされ、A = B = 2Cの関係が成り立つため、回転定数から1つの構造パラメーターしか決定できません。本研究では、超高分解能レーザー分光法によって正確に決定された回転定数値を用い、超高分解能レーザー分光法を補完するために、ab initio理論計算を利用することを試みました。一般にC-H結合長はC-D結合長よりも長いことが知られています。事実このH/Dの構造の違いはCH3O/CD3O分子における構造および回転定数の実験・計算の解析からも明らかになっています(J. Comput. Chem. Jap. 2016, 15, 199.)。ところが、もっとも単純な芳香族化合物であるC6H6およびその重水素置換体のC6D6分子の回転定数を精密に求めたところ、C6H6とC6D6では、C-H結合もC-D結合もほぼ同じ長さでした(図3)。芳香族炭化水素はいくつかのC-H結合を持っており、通常のC-H伸縮モードのほとんどには反対称運動が含まれます。 よって、振動平均化によるC-H結合の伸長は小さくなり、ベンゼンでは平均結合長に対する重水素の影響が小さいと考えられます。一方で、ベンゼン分子を非平面として考えた場合、C-HをC-Dにすると、平均結合長はわずかに短くなり、面外への傾きも小さくなることがわかりました(図4)。C-HをC-Dに置換した際の幾何学的構造の差はわずかではあるものの、この差が生体機能としての膜の透過、吸着、水素結合等の調整にどのように影響するかについては、さらなる研究が必要です(図5)。先生が主張する、「たかが0.015%、されど0.015% H/D」を実証できるような今後の展開が期待されます。

2,『核酸ナノメディシンの開発-重水素標識核酸によるセラノスティクスへの展開を目指して』 宮本 寛子 先生
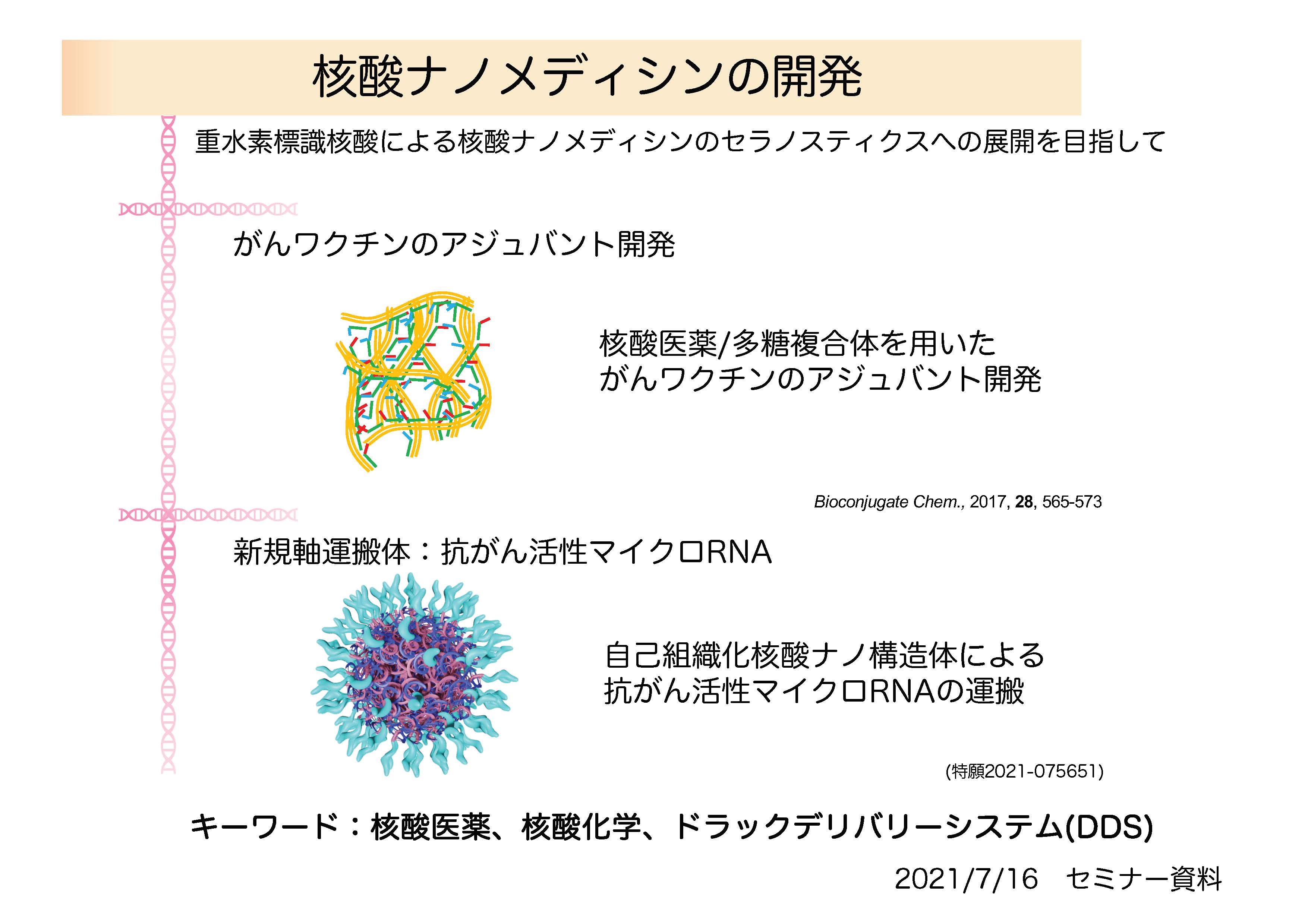
A01班 研究協力者の宮本 寛子先生は、北九州市立大学大学院で博士(工学)を取得され、現在は愛知工業大学工学部ゲノム創薬化学研究室で講師として研究に取り組んでおられます(図6)。本セミナーでは、『核酸ナノメディシンの開発-重水素標識核酸によるセラノスティクスへの展開を目指して』と題して、1)核酸診断技術:重水素標識核酸、2)がんワクチンのアジュバント開発、3)新規軸運搬体:抗がん活性マイクロRNA、に関して研究成果をご紹介いただきました(図7)。


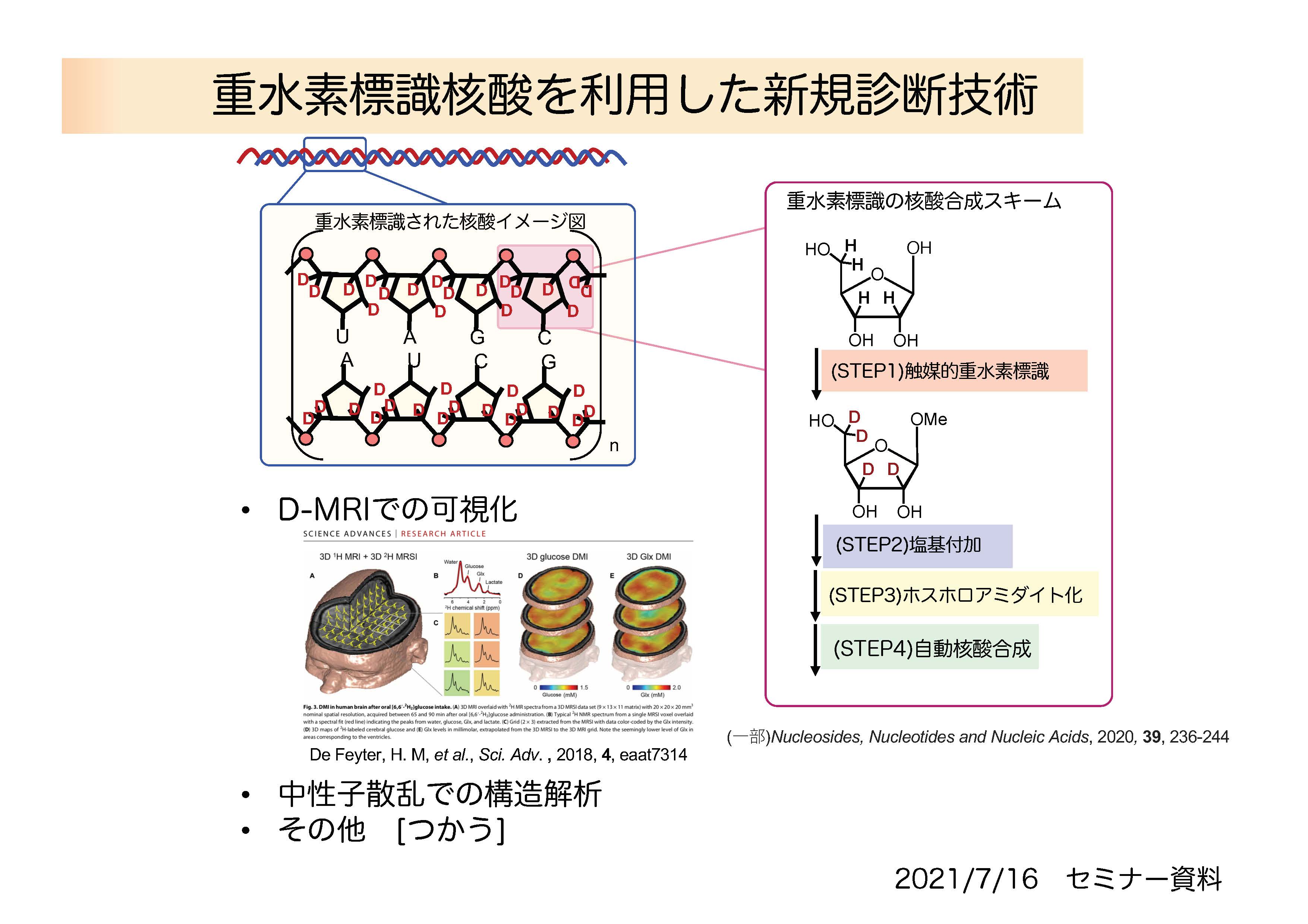
セラノスティクス (theranostics)とは「治療の」(therapeutic)と「診断の」(diagnostic)を組み合わせた造語で、診断と治療をあわせて行う考え方や、その手法のことをいいます。アンチセンスやsiRNAに代表される核酸医薬品は、これまで治療が難しかった遺伝性疾患や難治性疾患に対する新しいモダリティであり、セラノスティクスへの展開が可能です。従来、核酸は、蛍光標識や放射性同位元素で標識していましたが、重水素標識核酸を用いることで、D-MRIでの可視化や中性子散乱での構造解析等が可能になります。すでに重水素化グルコースは、癌細胞の有するワールブルク効果を利用した脳腫瘍の可視化に成功しています(Sci. Adv. 2018, 4, eaat7314.)(図8)。宮本先生らは、A01班研究代表者の澤間善成先生らと共同で、糖の部分を触媒的重水素標識した後、塩基を付加し重水素標識ヌクレオシドの合成を行っています。重水素標識核酸の研究から、核酸医薬品の有用性に関するブレイクスルーが生まれることが期待されます。
その他、核酸医薬/多糖複合体を用いたがんワクチンのアジュバント開発や自己組織化核酸ナノ構造体による抗がん活性マイクロRNAの運搬に関する研究成果をご紹介いただきました(図9)。