(プレスリリース)Iridium-catalyzed α-selective deuteration of alcohols

1.背景
重水素は天然に存在する非放射性の水素同位体であり、その質量差と量子効果から炭素−重水素結合 (C−D 結合) の切断には炭素−軽水素結合 (C−1H結合) の切断に比べ大きなエネルギーを要します。この、切断されにくい C−D 結合の特徴を利用して、医薬品の有効成分で代謝を受ける箇所の水素を重水素で置き換えた重医薬品(重水素化医薬品、重薬)の開発が進んでいます。重医薬品はもとの医薬品と比べて高い代謝安定性を示すことが予想されるため、代謝研究への利用や、副作用の少ない薬としての臨床応用などへの期待が高まっています。実際、2017年には FDA から重医薬品が新薬として承認されており、2022年現在も10 種類以上の候補化合物が臨床試験を実施しています(図1)。
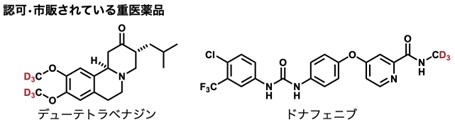
医薬分子に含まれるヒドロキシ基 α 位の炭素−水素結合 (C−H結合) は代謝による切断を受けやすい代表的な位置であるため、重水素化の魅力的な標的部位となっています。しかしながら、これまでヒドロキシ基 α 位のみを重水素化した医薬分子の合成には高価な重水素化試薬を利用した多段階合成を必要とするため、医薬分子に含まれるヒドロキシ基 α 位に対して効率的に重水素を導入することは困難でした。
この問題を解決するために、私たちは医薬分子の直接的なC(sp3)−H 結合重水素化反応に着目しました。医薬分子の直接的なC(sp3)−H 結合重水素化は、2017年に Prinston 大学の MacMillan 教授らによって提唱された新しいアプローチで、同教授らはアミノ基 α 位に対して有効な方法を報告しています。有機物質に含まれるヒドロキシ基 α 位の直接重水素化反応としては、これまでに遷移金属錯体触媒や不均一系触媒などの触媒と、重水 (D2O) を組み合わせて用いた反応がいくつか報告されていますが、さまざまな官能基をもつ医薬分子に広く適用可能なアルコールの α 位選択的な重水素化法は知られていませんでした。
そこで本研究では、ロサルタンカリウムに代表される医薬分子のヒドロキシ基 α 位を、重水を使って直接重水素化する触媒系の探索研究に取り組んだところ、機能性配位子(ビピリドナート配位子)をもつイリジウム触媒を用いれば、ロサルタンカリウムを含む幅広い種類のアルコールの直接重水素化が可能になることを明らかにしました(図2)。
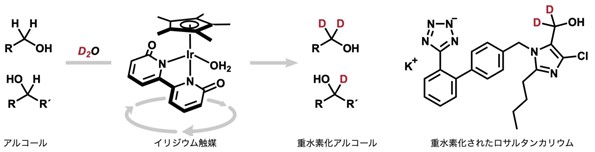
2.研究手法・成果
本研究では、2012 年に京都大学の藤田健一教授らによって開発されたイリジウム−ビピリドナート錯体に着目しました。この錯体は幅広いアルコールの脱水素化反応を効率よく促進します。アルコールの脱水素化触媒反応の反応過程では、イリジウムヒドリドとカルボニル化合物が生成することが提案されています。脱水素化反応ではこのイリジウムヒドリドが分解して水素ガスを発生してしまいますが、反応を閉鎖系で実施することで、イリジウムヒドリドが分解する前に重水と反応してイリジウムデューテリドを与え、イリジウムデューテリドがカルボニル化合物と反応すれば目的の重水素化アルコールが得られ、イリジウム触媒を再生すると考えました。
実際、ヒドロキシ基 α 位が代謝部位であることが知られるロサルタンカリウムを標的化合物として検討した結果、このイリジウム−ビピリドナート錯体触媒を用いることで、ロサルタンカリウムに含まれるヒドロキシ基 α 位水素のみを効率的に重水素化できることが分かりました(図3)。従来の触媒とは異なり、イミダゾールやテトラゾールなどの、医薬品によく含まれる配位性官能基の影響を受けることなく、ヒドロキシ基 α 位の重水素化のみが進行します。同様の塩基性あるいは中性条件下、様々な第一級アルコールと第二級アルコールの重水素化も進行することが分かりました。この方法によって、ラピドセプトやチロソール、グアイフェネシン、ジプロフィリンなどの医薬品や天然物の効率的重水素化も可能となりました(図4)。
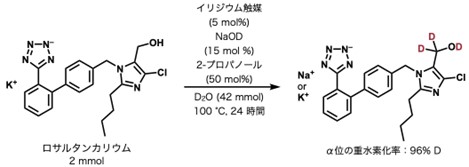
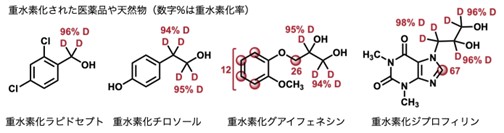
これまでこれらの重水素化されたアルコールは高価な重水素を含む還元剤などを用いて合成されていましたが、今回の方法では最も入手容易な重水を主な重水素源として合成できる点で、経済的に優れています。また、最終製品であるアルコールを原料として重水素化できるため、わざわざ重水素化アルコールを作るための新しい合成方法を考える必要がなく、既存の設備をそのまま使用することができます。
さらに、スペクトル実験や速度論実験、量子化学計算の結果から、このイリジウム触媒を用いたアルコールの重水素化反応が機能性ビピリドナート配位子とイリジウムの協奏効果を利用した 1) 脱水素化 2) H/D交換 3) 重水素化の 3 段階で進行していることが支持されました。この結果は、新しい重水素化反応を開発する上での触媒の設計指針を与えるものです。
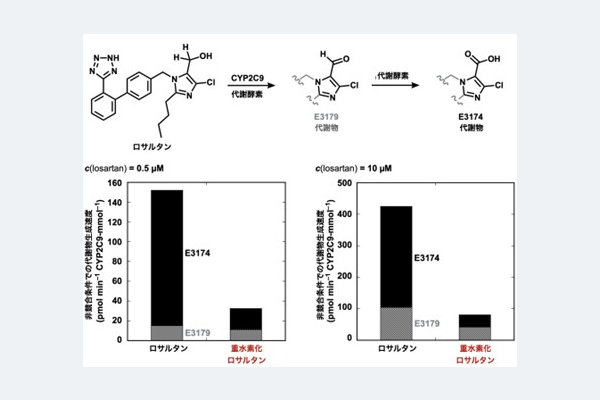
最後に、実際に重水素化した医薬品である重水素化ロサルタンの代謝安定性を評価したところ、ヒドロキシ基 α 位が重水素化されたロサルタンは、重水素化されていないロサルタンと比較して、代謝に対する安定性が大幅に向上していることが分かりました(図5)。このロサルタンのヒドロキシ基 α 位が重水素化による代謝安定性に対する知見は今回初めて得られたものであり、今後の重医薬品を開発するにあたって重水素に由来する速度論的同位体効果を活用するために重要な知見を与えるものと期待できます。
3.波及効果、今後の予定
今回、医薬品を含めた複雑なアルコールの直接重水素化技術を確立したことで、様々なアルコールに直接重水素を導入することが可能になりました。これにより、医薬品を含めた多くの機能性有機分子が示す本来の性質を損なうことなく、耐久性のみを上昇させる可能性が大きく広がりました。また、これまで主に sp2 炭素の重水素化に有効であると考えられていたイリジウム錯体も機能性ビピリドナート配位子と組み合わせることで、ヒドロキシ基 α 位を含めた sp3 炭素の重水素化が可能となったことから、機能性ビピリドナート配位子を利用した様々な金属錯体によって多様な有機物質の重水素化が可能になることが期待できます。これによって、今回の方法ではうまく重水素化できなかったアルコールや、アミンなどの官能基についても従来法とは相補的な重水素化技術を実現できることが期待されます。これによって、これまで不可能とされていた、ありとあらゆる有機材料の耐久性を合理的に高める技術開発が達成される可能性があります。
現在、学術変革領域研究(B)「重水素学」の窓口を通して、京都大学はこれらの成果を広く社会に提供すべく、技術提供や資料提供を進めています。
4.研究プロジェクトについて
本研究は、科研費助成金学術変革領域研究(B)「重水素学」(20H05739, 宇田川太郎; 20H05740, 中寛史; 20H05741, 前川京子)、科研費助成金基盤研究 C(21K04991, 宇田川太郎)ならびにAMED-BINDS 「精密合成技術に基づくハイブリッド型ニューモダリティ創製の創薬支援」(竹本佳司)の支援によって実施されました。
<研究者のコメント>
医薬品の重水素化は2017年に始まったばかりの新しい研究領域です。あらゆる医薬分子に水素原子が含まれていることを鑑みれば、これらの水素を合理的に重水素に置き換えることで医薬品の機能を最大限に発揮することが期待されます。今後も私たちは重水素で分子設計を変える「デュースイッチ(Deut-Switch)」研究を進めます。

